CTP FERNANDO VOLIO JIMÉNEZ
TAREA DE
QUÍMICA
TEMA:
ENLACES QUÍMICOS
DOCENTE:
LIC. EMILIANO MURILLO
SECCIÓN
11-4 B
ESTUDIANTE:
Juan Josè Rojas Obando
COSTA RICA, CARTAGO -2022
CTP FERNANDO VOLIO JIMÉNEZ
TAREA DE
QUÍMICA
TEMA:
ENLACES QUÍMICOS
DOCENTE:
LIC. EMILIANO MURILLO
SECCIÓN
11-4 B
ESTUDIANTE:
Juan Josè Rojas Obando
COSTA RICA, CARTAGO -2022
Doble. Los átomos enlazados aporta cada uno dos electrones de su última capa de energía, formando un enlace de dos pares de electrones. Se representa por dos líneas paralelas, una arriba y una abajo, similar al signo matemático de igualdad. Por ejemplo: O=O (Oxígeno-Oxígeno), O=C=O (Oxígeno-Carbono-Oxígeno).

Los enlaces metálicos son, como su nombre lo indica, un tipo de unión química que se produce únicamente entre los átomos de un mismo elemento metálico. Gracias a este tipo de enlace los metales logran estructuras moleculares sumamente compactas, sólidas y resistentes, dado que los núcleos de sus átomos se juntan a tal extremo, que comparten sus electrones de valencia.

Son enlaces que se forman cuando se comparten un, dos o mas pares de electrones entre dos o màs àtomos. Este enlace ocurre entre no metales.
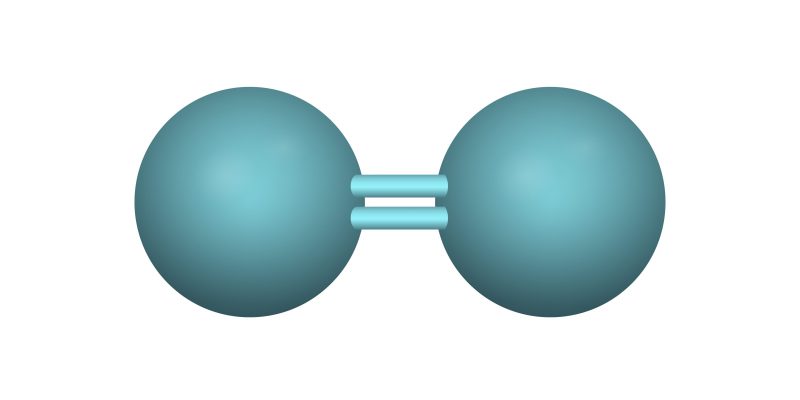
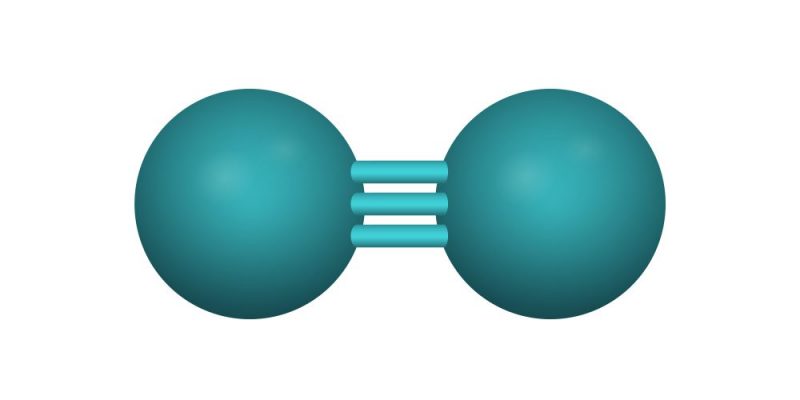
Ejemplos sencillos de enlace covalente son los que se dan en las siguientes moléculas:
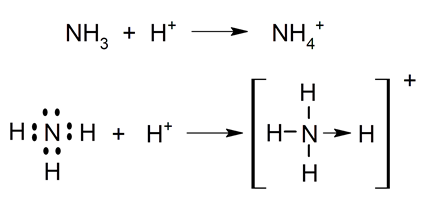
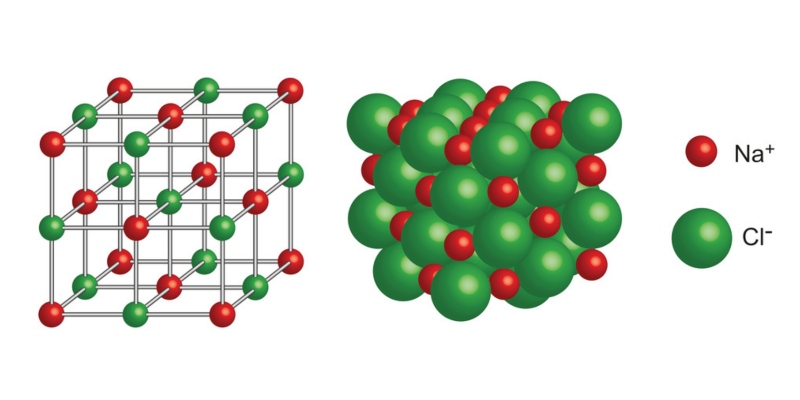
Este tipo de enlace se manifiesta generalmente entre átomos metálicos y no metálicos en los que la transferencia de electrones ocurre desde los átomos metálicos (menos electronegativos) hacia los no metálicos (más electronegativos).
Algunas características generales de un compuesto iónico: